Общая антиоксидантная способность (Т-АОС) Набор для анализа
Примечание: Перед тестированием возьмите два или три разных образца для прогнозирования..
Операционное оборудование: Спектрофотометр
Кот нет: BC1310
Размер:50Т/48С
Компоненты:
Экстракт раствора: Жидкость 50 мл×1. Хранение при 4℃, precool before use.
Реагент I: Жидкость 35 мл×1. Хранение при 4℃.
Реагент II: Жидкость 20 мл×1. Storage at 4℃ in shadow.
Реагент III: Жидкость 5 мл×1. Storage at 4℃ in shadow.
Стандартный: Порошок×1, 10 mg of FeSO4·7H2O. Рабочее решение: добавлять 0.9 mL of distilled water and 20μL of concentrated sulfuric acid (H2SO4) to forms 40 µmol/mL FeSO4 standard solution. Solution mixture (prepare when the solution will be used): Реагент I : Реагент II: Reagent III= 7:1:1, incubate at 37℃ before use.
Описание продукта:
This kit is used to detect the total antioxidant levels of antioxidants and antioxidant enzymes in the samples. It is mainly used in the study of biological, medical and pharmaceutical studies to detect the total antioxidant capacity of antioxidant solutions.
In acid environment, Fe3+ -TPTZ are reduced to blue Fe2+ -TPTZ. The color reaction reflects the total antioxidant capacity.
Требуемые реагенты и оборудование, которые не входят в комплект поставки:
Спектрофотометр, constant temperature water bath, low temperature centrifuge, 1 mL glass cuvette and distilled water.
Процедура:
я. Базовые приготовления:
1. сыворотка, плазма, слюна, or urine samples
Плазма (anticoagulation with heparin or sodium citrate, avoid using EDTA), центрифуга в 5000 rpm/min for 10 мин, take supernatant for test. Take serum, saliva or urine samples for direct determination. Also, you can store at -80℃ and detect within 30 дни.
2. Cells or tissue образец
Брать 1-2 million cells or 0.1 г ткани, добавлять 1.0 mL of Extract solution. Use homogenate or ultrasound to fully break up cells and release antioxidant, центрифуга в 10000 r/min and 4℃ for 5 мин, take supernatant for test. Measure the concentration of protein if needed.
II. Determination procedure:
- Разбавить 40 μmol/mL FeSO4 standard solution to 0.1, 0.05, 0.025, 0.0125, 0.00625, 0.003125 мкмоль/мл, брать 500 μL of standard solution (distilled water for blank control), add to 500 мкл реагента II. Mix thoroughly for 10 мин, detect the absorbance in 593 нм, calculate ΔA=AS-AB. (КАК: standard solution tube, АБ: blank control tube.) The final concentration of Fe2+ is 0.05、0.025、0.0125、0.00625、
0.003125、0.00156 мкмоль/мл.
- Preheat the spectrophotometer 30 мин, отрегулировать длину волны, чтобы 593 nm and set zero with distilled
- Добавьте реагенты из следующего списка:
| Название реагента | Пустая трубка (АБ) | Пробирка (В) |
| Solution mixture (мкл) | 900 | 900 |
| Образец (мкл) | 30 | |
| Double distilled water (мкл) | 120 | 90 |
| Mix thoroughly and react for 10 мин, установить ноль с помощью дистиллированной воды, detect the absorbance in 593 нм. Calculate ΔA’=AT – АБ. (Примечание: The blank tube just needs to be tested once or twice in every experiment) | ||
III. Расчет:
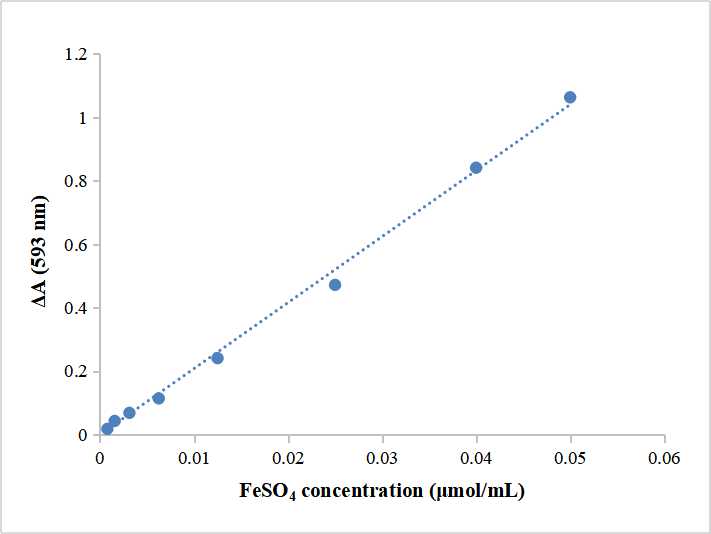
- Создать стандартную кривую
Take the Fe2+ final concentration as X-axis, △A as Y-axis, create standard curve, get linear regression equation y=kx+ b, take ΔA’ into the equation to get x (мкмоль/мл).
- Определение единицы измерения: the sample antioxidant capacity is indicated by the standard liquid ion concentration required for the same absorbance change(ΔА).
А. Белок концентрация:
Общая антиоксидантная способность (мкмоль/мг прот) = x × Vrv÷ (Vs× Cpr) = 34× x ÷ Cpr
Б. Образец weight
Общая антиоксидантная способность (μmol/g weight) = x × Vrv÷ (Vs ÷ Vsv ×W) =34× x÷ W
С. Клетка amount
Общая антиоксидантная способность (μmol/104cell) = x × Vrv÷ (Vs ×Vsv÷n) = 34× x÷ n
Д. Решение объем
Общая антиоксидантная способность (мкмоль/мл) =x× Vrv÷ Vs =34×x
Веревка: total reaction volume, 1.02 мл; Против: объем пробы, 0.03 мл;
Всв: объем добычи, 1 мл; Вт: sample weight, г;
КПР: концентрация белка в образце, мг/мл;
н: cell amount, unit based on 104 (ten thousand).
Примечание:
- Reagent II is irritated to human body, please wear lab clothes and latex
- The samples should not be appeared blue under acidic condition, or it will interference sample result of the
- Detergent such as Tween, Triton, NP-40 and reductants such as DTT, mercapto ethanol should not be added in the
- If the absorbance value determined by the sample is beyond the standard curve range, the sample should be diluted or concentrated properly before
- The kit should be store at2-8℃.
Примеры:
- Add 0.1g shamrock to 1mL extract solution and grind thoroughly on ice, take supernatant, follow the determination procedure to operate, with 96-well flat-bottom plates to calculate: ΔA=A(Т)-А(Б)=0.909-0.148=0.761, standard curve: y=21.056x-0.0087, calculate x=0.037, according to mass of sample to calculate Total antioxidant capacity (μmol/g mass) =34×x÷W=34×0.037÷0.1=12.85 μmol/g mass.
Рекомендации:
[1] Pellegrini N, Serafini M, Salvatore S, и другие. Total antioxidant capacity of spices, dried fruits, nuts,
pulses, cereals, and sweets consumed in Italy assessed by three different in vitro assays[Дж]. Molecular nutrition & food research, 2006, 50(11): 1030-1038.
сопутствующие товары:
BC1320/BC1325 Hydroxyl Radical Scavenging Capacity Assay Kit
BC1330/BC1335 Plant Flavonoids Assay Kit
BC1340/BC1345 Plant Total Phenol (TP)Набор для анализа
BC1350/BC1355 Plant Proanthocyanidins Assay Kit


Отзывы
Отзывов пока нет.